1. ĐẶC ĐIỂM HÌNH THÁI:1.1. Nhuộm Gram (phương pháp Hucker cải tiến) Vật liệu, hoá chất: · Dung dịch Tím kết tinh (Crystal violet): 2g tím kết tinh hoà tan trong 20 ml etanol 95% 0,8 g ammon oxalat hoà tan trong 80 ml nước cất Trộn hai dịch nói trên lại với nhau, giữ 48 giờ rồi lọc. Bảo quản trong lọ tối, sử dụng vài tháng. · Dung dịch Iod: Hoà tan 1 g Iod (Iodine) trong 3-5ml nước cất, thêm 2g KI (Kali iodide), khuấy cho tan hết, thêm nước cất cho đủ 300ml. Bảo quản trong lọ tối. · Dung dịch tẩy màu: Etanol 95% hoặc trộn hỗn hợp 70ml etanol 95% với 30ml aceton. · Dung dịch nhuộm bổ sung: Chuẩn bị sẵn dung dịch Safranin O 2,5%, trước khi dùng pha với nước cất theo tỷ lệ 1:5 (vol/vol) để có dung dịch 0,5%. Các bước tiến hành:· Chuẩn bị vết bôi: dùng que cấy vô trùng lấy một ít vi khuẩn từ thạch (sau khi cấy 24 giờ) hoà vào 1 giọt nước cất ở giữa phiến kính, làm khô trong không khí. · Cố định tế bào: hơ nhanh vết bôi trên ngọn lửa đèn cồn 2-3 lần. · Nhuộm bằng dung dịch Tím kết tinh trong 1 phút, rửa nước, thấm khô. · Nhuộm lại bằng dung dịch Iod trong 1 phút, rửa nước, thấm khô. · Nhỏ dịch tẩy màu, giữ khoảng 30 giây (cho đến khi vừa thấy mất màu), rửa nước, thấm khô. · Nhuộm bổ sung bằng dung dịch Safranin trong 2-3 phút, rửa nước, để khô trong không khí. · Soi kính: dùng vật kính dầu 100´. Kết quả:Vi khuẩn Gram (+) bắt màu tím, Gram (-) bắt màu đỏ.
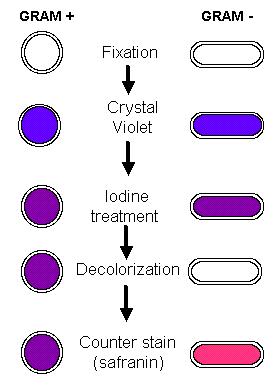
Hình 1.1. Các bước tiến hành nhuộm Gram và ví dụ minh hoạ kết quả. 1.2. Nhuộm tiên maoVật liệu, hoá chất:· Dung dịch A: Acid tannic 5 g FeCl3 1,5 g Formalin 2 ml NaOH 1% 1 ml Nước cất 100 ml · Dung dịch B: 2 g AgNO3 hoà tan trong 100 ml nước cất, lấy 10 ml dể riêng. Nhỏ dung dịch NH4OH đậm đặc vào 90 ml còn lại, thấy hình thành tủa rất đặc, tiếp tục nhỏ NH4OH vào cho đến khi tan hết tủa. Lấy 10ml AgNO3 đã bỏ ra ban đầu nhỏ từ từ vào dung dịch, thấy xuất hiện váng mỏng, tiếp tục nhỏ vào cho đến khi vừa tan hết váng thì thôi. · Chuẩn bị phiến kính: rửa thật sạch, ngâm trong cồn, đốt cháy hết cồn rồi mới sử dụng. Các bước tiến hành:· Hoạt hoá vi khuẩn 2-3 lần trước khi tiến hành nhuộm. · Dùng que cấy vô trùng lấy vi khuẩn từ mặt thạch (mới cấy 18-24 giờ) hoà vào 1 giọt nước cất đặt giữa phiến kính, để nghiêng cho chảy về một phía, làm khô trong không khí. · Cố định tế bào: hơ nhanh trên ngọn lửa đèn cồn 2-3 lần. · Nhỏ dịch A lên vết bôi, giữ 10 phút, rửa bằng nước cất. · Dùng dịch B cho chảy qua để loại hết nước. Nhuộm bằng dịch B trong 30-60 giây. Hơ nóng, để nguội rồi rửa lại bằng nước cất. · Soi kính: dùng vật kính dầu 100´. Kết quả:Tế bào vi khuẩn bắt màu nâu thẫm, tiên mao bắt màu nâu.
Hình 1.2. Ví dụ minh hoạ kết quả nhuộm tế bào vi khuẩn và tiêm mao 1.3. Kiểm tra khả năng di độngVật liệu, hoá chất:· Chuẩn bị ống nghiệm chứa môi trường thạch bán lỏng (0,3-0,6% thạch). Các bước tiến hành:· Dùng que cấy có đầu nhọn cấy vi khuẩn theo kiểu chích sâu vào môi trường thạch bán lỏng. · Đặt ống nghiệm thẳng đứng, ủ ở nhiệt độ thích hợp và quan sát sau 1-3 ngày, có khi lâu hơn. Kết quả:Vi khuẩn mọc lan rộng quanh vết cấy tức là chúng có khả năng di động. Vi khuẩn chỉ mọc theo vết cấy tức là chúng không có khả năng di động Chú ý: với vi khuẩn hiếu khí chỉ quan sát ở phần trên của vết cấy. 1.4. Nhuộm bào tửCó hai phương pháp nhuộm 1.4.1. Nhuộm Lục Malachit (phương pháp Schaeffer-Fulton)Vật liệu, hoá chất:· Dung dịch Lục Malachite (Malachite green) bão hoà (khoảng 7,6%) · Dung dịch Safranin 0,5% (xem nhuộm Gram) Các bước tiến hành:· Làm vết bôi và cố định tế bào như đối với nhuộm Gram. · Nhuộm bằng dung dịch Lục Malachite trong 10 phút, rửa nước. · Nhuộm lại bằng dung dịch Safranine trong 30 giây, rửa nước, thấm khô. · Soi kính: dùng vật kính dầu 100´ Kết quả:Bào tử có màu lục, tế bào có màu đỏ. Chú ý: phân biệt bào tử với các hạt dị nhiễm cũng bắt màu lục 1.4.2. Nhuộm Carbolic FuchsinVật liệu, hoá chất:· Dung dịch A: 10 ml dung dịch Fuchsin kiềm bão hoà trong etanol (khoảng 10%) 100 ml dung dịch acid carbolic (phenol) 5% (trong nước). Trộn đều với nhau (chuẩn bị trước khi dùng) · Dung dịch B: 100 ml Etanol 95% 3 ml HCl đậm đặc · Dung dịch C: 30 ml dung dịch Xanh metylen (Methylene blue) bão hoà trong etanol (khoảng 2%) 100 ml dung dịch KOH 0,01% trong nước. Trộn đều với nhau, để càng lâu càng tốt. Các bước tiến hành:· Làm vết bôi trên phiến kính, cố định tế bào. · Nhỏ dung dịch A lên vết bôi, hơ nóng nhẹ bên dưới để bay hơi, tránh để sôi. Thêm dần dần thuốc nhuộm để không bị khô cạn, giữ trong 5 phút. Đợi nguội, đổ thuốc nhuộm đi. · Dùng dịch B rửa cho đến khi vừa thấy vừa hết màu đỏ, rửa nước. · Nhuộm lại bằng dung dịch B trong 2-3 phút, rửa nước, thấm khô. · Soi kính: dùng vật kính dầu. Kết quả:Bào tử bắt màu đỏ, tế bào bắt màu xanh
Hình 1.3. Các bước tiến hành nhuộm Carbolic Fuchsin và ví dụ minh hoạ kết quả.
1.5. Nhuộm vỏ nhầy (Capsule)Có hai phương pháp 1.5.1. Phương pháp nhuộm âm bảnVật liệu, hoá chất:· Mực tàu · Metanol · Dung dịch safranin 0,5% Các bước tiến hành:· Lấy vi khuẩn hoà vào giọt nước trên phiến kính. · Nhỏ thêm 1 giọt mực tàu, trộn đều. Dùng cạnh lamen dàn mỏng vết bôi, làm khô trong không khí. · Cố định vết bôi bằng cách nhỏ metanol lên vết bôi, giữ trong 1 phút. · Thêm dần dần dung dịch Safranin 0,5% lên vết bôi để rửa metanol, sau đó giữ trong 30 giây để nhuộm lại, rửa nước, thấm khô. · Soi kính: dùng vật kính dầu 100´. Kết quả:Nền vi trường màu đen, tế bào màu đỏ, vỏ nhầy màu hồng. 1.5.2. Phương pháp Đỏ CongoVật liệu, hoá chất:· Dung dịch Đỏ Congo (Congo red) 2% trong nước · Dung dịch gelatin 0,01-0,1% trong nước · Dung dịch HCl 1% · Hỗn hợp 30 ml dung dịch Xanh metylen bão hoà (khoảng 2%) trộn với 100 ml dung dịch KOH 0,01%. Các bước tiến hành:· Nhỏ 1 giọt dung dịch Đỏ Congo và 1 giọt dung dịch gelatin lên phiến kính sạch. · Lấy vi khuẩn trộn đều với 2 giọt nói trên để làm vết bôi, để khô trong không khí · Nhỏ dung dịch HCl lên để rửa, phiến kính có màu xanh. · Rửa bằng nước để loại bỏ dung dịch HCl. · Nhuộm lại bằng Xanh metylen trong 1 phút, rửa nước, hong khô. · Soi kính: dùng vật kính dầu 100´. Kết quả:Nền vi trường màu xanh, tế bào màu đỏ, vỏ nhầy không màu 1.5.3. Phương pháp nhuộm âm bản đơn giản (Hình 1.4): · Nhỏ 1 giọt Nigrosin vào đầu một phiến kính sạch. · Lấy 1 vòng que cấy vi khuẩn trộn với giọt nigrosin. · Lấy một phiến kính khác để nghiêng 450 và kéo giọt nigrosin đã trộn vi khuẩn về phía phải một chút sau đó kéo nhẹ về phía trái để dàn mỏng thành một vết bôi. Để khô tự nhiên (không hơ lửa). · Quan sát dưới kính hiển vi sẽ thấy vỏ nhầy màu sáng nổi lên trên một nền màu đen.
Hình 1.4. Nhuộm âm bản dùng Nigrosin và ví dụ minh hoạ kết quả.
1.5.4. Phương pháp dùng Tím kết tinh (Crystal violet)Vật liệu, hoá chất:· Dung dịch Tím kết tinh 1% trong nước · Dung dịch Sulfat đồng CuSO4 20% trong nước Các bước tiến hành:· Nhỏ vài giọt dung dịch tím kết tinh lên phiến kính sạch · Lấy vi khuẩn từ ống thạch nghiêng (48 giờ) trộn với dung dịch tím kết tinh, dùng cạnh lam kính dàn đều trên toàn bộ phiến kính để làm vết bôi, giữ trong không khí 5-7 phút để làm khô, không được hơ nóng. · Rửa vết bôi bằng dung dịch sulfat đồng 20%, thấm khô. · Soi kính: dùng vật kính dầu 100´. Kết quả:· Tế bào có màu sẫm, vỏ nhày màu nhạt ở xung quanh. 1.6. Nhuộm thành tế bàoVật liệu, hoá chất:· Dung dịch acid tannic 5% · Dung dịch Tím kết tinh 0,2% Các bước tiến hành:· Làm vết bôi vi khuẩn · Nhuộm bằng dung dịch acid tannic trong 5 phút, rửa nước. · Nhuộm bằng dung dịch Tím kết tinh trong 3-5 phút, rửa nước, thấm khô. · Soi kính: dùng vật kính dầu 100´ Kết quả:· Thành tế bào bắt màu tím, tế bào chất màu tím nhạt. 1.7. Nhuộm hạt dị nhiễmVật liệu, hoá chất:· Dung dịch A: Xanh Toluidin (Toluidine blue) 0,15 g Lục malachite 0,2 g Acid acetic (glacial) 1 ml Ethanol 95% 2 ml Nước cất 100 ml · Dung dịch B: Iod (I) 2 g Iodid kali (IK) 3 g Nước cất 300 ml Các bước tiến hành:· Làm vết bôi, cố định vết bôi. · Nhuộm bằng dịch A trong 5 phút, đổ đi · Tráng bằng dịch B, nhuộm thêm trong 1 phút, rửa nước, thấm khô. · Soi kính: dùng vật kính dầu 100´. Kết quả:Các hạt dị nhiễm có màu đen. Các thành phần khác của tế bào bắt màu lục hay lục nhạt 1.8. Nhuộm hạt PHB (Poly-β-hydroxybutyric acid)Vật liệu, hoá chất:· Dung dịch A: Đen Sudan B (Sudan black B) 0,3 g Etanol 70% 100 ml. Trộn đều, lắc mạnh, để qua đêm mới sử dụng. · Dung dịch B: Xylene · Dung dịch C: Dung dịch Safranin 0,5% trong nước. Các bước tiến hành:· Làm vết bôi, cố định vết bôi. · Nhuộm bằng dịch A trong 10 phút, rửa nước, thấm khô. · Dùng dịch B rửa cho đến khi mất màu. · Nhuộm bằng dịch C trong 1-2 phút, rửa nước, thấm khô. · Soi kính: dùng vật kính dầu 100´ Kết quả:Hạt PHB bắt màu lam đen. Tế bào và các bộ phận khác có màu đỏ. 1.9. Nhuộm tinh thể protein (ở Bacillus thuringiensis)Vật liệu, hoá chất:· Dung dịch nhuộm: 1 ml dung dịch Fuchsin bão hoà bão hoà (xem nhuộm carbolic fuchsin) trộn với 100 ml dung dịch acid carbolic 5% trong nước. Khi dùng pha loãng 10 lần. Các bước tiến hành:· Làm vết bôi, cố định vết bôi · Nhuộm trong 1 phút, rửa nước, hong khô · Soi kính: dùng vật kính dầu Kết quả:Tinh thể bắt màu đỏ. Bào tử tách rời có vòng màu đỏ 1.10. Nhuộm vi khuẩn kháng acidVật liệu, hoá chất:· Dung dịch A: Dung dịch Fuchsin kiềm bão hoà trong nước (» 10%) 10 ml Dung dịch acid carbolic 5% trong nước 100 ml Trộn đều 2 dung dịch với nhau. · Dung dịch B: Etanol 95% 100 ml HCl đặc 3 ml · Dung dịch C: Dung dịch Xanh metylen bão hoà trong etanol (» 2%) 30 ml Dung dịch KOH 0,01% trong nước 100 ml Các bước tiến hành:· Làm vết bôi, cố định · Nhỏ dịch A lên vết bôi, đun nhẹ dưới phiến kính cho bay hơi nhưng không sôi. Thường xuyên bổ sung thêm dịch A để tránh khô vết bôi. Giữ trong 5 phút. Đợi nguội, đổ dịch A đi. · Dùng dịch B rửa cho đến khi thấy vừa mất màu đỏ. Rửa nước kỹ. · Nhuộm bằng dịch C trong 2-3 phút, rửa nước, thấm khô. · Soi kính: dùng vật kính 40´ Kết quả:Vi khuẩn kháng acid bắt màu đỏ. Vi khuẩn không kháng acid bắt màu xanh.
Hình 1.5. Ví dụ minh hoạ kết quả xác định tính kháng acid của vi khuẩn.
2. ĐIỀU KIỆN NUÔI CẤY VÀ ĐẶC ĐIỂM SINH LÝ:2.1. Hình thái khuẩn lạc· Lấy 15-20ml môi trường thạch vô trùng, để nguội đến 50 0C rồi đổ vào đĩa Petri (thao tác vô trùng). Nếu có nước ngưng tụ trên nắp hộp cần úp ngược xuống để vào tủ ấm 30-37 0C để làm khô mặt thạch. · Lấy một vòng que cấy gạt 3-4 lần trên mặt thạch ở một góc. Quay đĩa thạch sang hướng khác và ria cấy từ một vạch thành 3-4 đường khác sao cho không trùng với các đường trước. Lặp lại theo một hướng thứ ba để pha loãng hơn nữa phần vi khuẩn dính trên que cấy. Chú ý không nhấc tay lên và không thay đổi hướng của vòng que cấy. · Đặt vào nhiệt độ thích hợp trong 1-2 ngày để chọn ra các khuẩn lạc mọc riêng rẽ. · Tiến hành quan sát các khuẩn lạc này từ các phía (từ trên xuống, từ bên cạnh), chú ý về kích thước, hình dạng khuẩn lạc, hình dạng mép, bề mặt, độ dày, có núm hay không, độ trong, màu sắc (trên, dưới, có khuếch tán ra môi trường hay không)
Hình 2.1. Cấy ria tế bào để tách khuẩn lạc đơn và các dạng khuẩn lạc thường gặp. 2.2. Nhiệt độ sinh trưởng và tính bền nhiệt· Lấy một vòng que cấy sinh khối cấy vào các ống nghiệm có môi trường dinh dưỡng thích hợp (môi trường thạch hoặc dịch thể). · Đặt ở các điều kiện nhiệt độ khác nhau (3 ống trong một nhiệt độ). Đối với các loài ưa ấm (mesophiles), nhiệt độ sinh trưởng và tính bền nhiệt thường được kiểm tra với thang nhiệt độ 4, 20, 30, 37, 41, 45 và 65 0C. Từ 37 0C trở lên có thể dùng các nồi cách thủy ổn nhiệt. · Quan sát khả năng sinh trưởng của vi khuẩn (tạo sinh khối trên môi trường thạch, hoặc đo OD nếu thí nghiệm được tiến hành trên môi trường dịch thể) Đặc biệt, tính bền nhiệt cần xác định khi phân loại các Liên cầu khuẩn, cách làm như sau: · Cấy 1 giọt dịch nuôi cấy 24 giờ vào ống nghiệm đựng môi trường dịch thể thích hợp. · Giữ ở nồi cách thủy 60 0C trong 30 phút sau đó đặt vào tủ ấm 35-37 0C, nuôi trong 48 giờ. Nếu vi khuẩn phát triển được là có tính bền nhiệt. Dùng chủng vi khuẩn Enterococcus faecalis làm đối chứng dương tính.
|
© http://vietsciences.free.fr , http://vietsciences.org
, http://vietsciences2.free.fr Nguyễn Lân Dũng